Модель, созданная из клеток пациента, воспроизводит повреждения, наблюдаемые при мышечной дистрофии Дюшенна.
С использованием клеток пациента ученые создали трехмерную (3D) модель искусственной мышцы, которая точно воспроизводит повреждения, наблюдаемые у людей с мышечной дистрофией Дюшенна (МДД).
Новая модель, по мнению ученых, позволит более эффективно тестировать методы лечения, которые потенциально могут обратить вспять повреждение клеток.
Результаты описаны в исследовании «Сарколеммное повреждение in vitro: сократительная 3D-модель скелетной мышцы для тестирования препаратов лечения мышечной дистрофии Дюшенна», опубликованном в журнале Biofabrication.
Команда уже планирует разработать усовершенствованную версию 3D-модели мышц, включающую дополнительные технологии, которые могли бы ускорить тестирование потенциальных методов лечения.
«Мы гордимся тем, что осуществляли финансирование проекта, который может ускорить исследовательский процесс за счет создания модели «орган-на-чипе»,
— Сильвия Авила, президент проекта для родителей детей с МДД в Испании, который финансировал исследование, — говорится в пресс-релизе.
«С одной стороны, мы сокращаем число лабораторных опытов над животными, а с другой стороны, время, чтобы воплотить потенциальную терапию в реальность. Это имеет решающее значение для болезни, которая отнимает у наших детей время и качество жизни»,
— добавил Авила.
Ученые впервые смоделировали первопричину МДД
При мышечной дистрофии Дюшенна, наиболее распространенном типе мышечной дистрофии, мутация в гене вызывает недостаток выработки дистрофина — белка, который помогает защитить мышечные клетки от износа. Таким образом, у пациентов наблюдается прогрессирующая атрофия мышц.
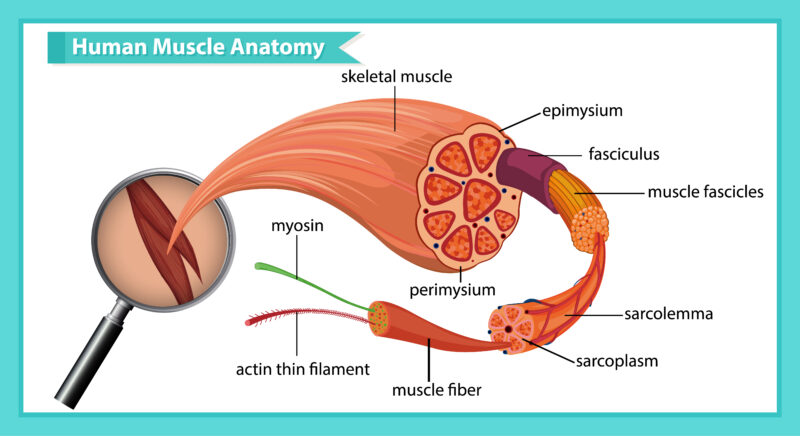
В частности, недостаток дистрофина вызывает хрупкость сарколеммы — мембраны мышечных клеток, что приводит к повреждению мышечных волокон при их сокращении.
Одной из проблем при разработке методов лечения МДД является отсутствие доклинических инструментов, позволяющих моделировать сложность заболевания.
3D-модель, созданная с использованием клеток пациента, является многообещающим подходом для более точного моделирования состояния человека. Эта искусственная, но функциональная ткань будет иметь те же клеточные характеристики, что и у пациента, от которого они были получены.
Теперь, используя клетки пациентов с МДД, группа ученых успешно разработала искусственную трехмерную модель. Сконструированные мышцы обладают сократительной функциональностью и реагируют на электроимпульсную стимуляцию.
Важно отметить, что длительные режимы сокращения вызывали повреждение сарколеммы, что отражает потерю целостности мышечных волокон, обычно наблюдаемую у пациентов с МДД. Между тем, в мышцах, созданных из здоровых клеток, таких повреждений не наблюдалось.
«Мы долго работали над разными протоколами, пока нам не удалось добиться того, чтобы это повреждение появилось в клетках пациентов, но не в контрольных клетках людей без Дюшенна», —
сказала Айноа Техедера-Виллафранка, аспирантка Института биоинженерии в Каталонии (IBEC), Испания, и первый автор исследования.
«Это деликатно, потому что, если вы стимулируете мышцу, вы также можете вызвать разрыв волокон в здоровых клетках, так же, как это происходит, когда мы занимаемся спортом и испытываем мышечные боли»,
— добавляет Айноа Техедера.
После того, как повреждение было вызвано, мышечные ткани с МДД проявляли тенденцию к утомлению при повторной стимуляции, что указывает на то, что сарколеммальное повреждение ставит под угрозу функцию мышц, как это происходит в организме человека.
«Новизна этого исследования заключается в нашей попытке смоделировать первопричину заболевания, которой является повреждение сарколеммы», — говорит Хуанма Фернандес, доктор философии, старший научный сотрудник IBEC и старший автор исследования.
«Нам было крайне важно повторить это в лаборатории, и мы успешно это сделали. Раньше этого не делалось».
Новая 3D-модель мышц уже используется в лаборатории
Теперь исследователи надеются, что эту модель можно будет использовать для определения потенциальных методов лечения повреждения мышц, вызванного МДД. На сегодняшний день большинство методов лечения могут только облегчить симптомы.
Эта возможность уже была оценена командой, которая лечила мышечные клетки с помощью терапии повышения уровня атрофина, белка со структурой и функцией, сходной с дистрофином, который был идентифицирован как возможный инструмент лечения МДД.
Однако было обнаружено, что небольшие молекулы галофугинона или эзутромида оказывают эффект, противоположный желаемому. В частности, сократительная функция мышц была заметно снижена. Более того, галофугинон вызывал мышечную атрофию.
По словам исследователей, эти результаты согласуются с результатами предыдущих исследований терапии второй фазы, которые не показали эффективности.
Было обнаружено, что другой исследовательский активатор атрофина (от SOM Innovation Biotech – частная фармацевтическая компания) усиливает мышечные сокращения, но не защищает от повреждения сарколеммы.
«В целом эти результаты подчеркивают потенциал нашей модели в качестве базы для более глубокого понимания того, как потенциальные лекарства и другие молекулы могут влиять на функциональность скелетных мышц»,
— пишут исследователи.
Сейчас ученые работают над усовершенствованной моделью «орган-на-чипе», которая будет включать датчики и другие технологии, позволяющие лучше контролировать повреждение клеток, что еще больше ускоряет тестирование терапевтических молекул.
Команда продолжает работать с родителями детей с диагнозом МДД через проект Duchenne Parent Project Spain, некоммерческую организацию, которая финансирует исследование.
Фернандес-Коста говорит, что такое сотрудничество «является фантастическим примером того, как исследователи могут работать вместе с пациентами и их семьями для достижения общих целей».
Дата публикации статьи в источнике 5 октября 2023 г.
Автор перевода: Дунаева Елена — волонтер проекта ProCharity
Об авторе статьи
Линдси Шапиро, доктор философии, получила докторскую степень по нейробиологии в Университете Эмори в Атланте, где изучала новые терапевтические стратегии для устойчивых к лечению формам эпилепсии. За это исследование в 2019 году она была удостоена стипендии Американского общества эпилепсии. Линдси также ранее работала постдокторантом, изучая роль воспаления в развитии эпилепсии и болезни Альцгеймера.