Здоровую версию гена FKRP доставили путем внутривенного введения AB-1003.
Первый человек с ПКМДR9 получил генную терапию AB-1003 при участии в клиническом испытании, согласно заявлению разработчика терапии Asklepios BioPharmaceutical (AskBio).
Получение лечения в рамках испытания LION-CS101 еще один пример, как AskBio успешно предоставляет генную терапию своим кандидатам. В данном случае речь идет о препарате AB-1003. Это результат процесса — от публикаций на стендах до непосредственно клинических разработок,»
— Jude Samulski, кандидат наук, сооснователь и главный научный сотрудник в AskBio, сообщил в пресс-релизе.
Появление терапии AB-1003 — волнующий момент для ПКМД-сообщества
Осознание того, что первый пациент получил лечение в рамках испытаний AB-1003, действительно волнующий момент для сообщества ПКМД и всех, кто живет с таким изнурительным заболеванием,»
— Kelly Brazzo, сооснователь и директор некоммерческой организации CureLGMD2i, поделилась своими эмоциями.
«Учитывая отсутствие в настоящее время модифицирующей терапии для ПКМД, многие специалисты знают о возможностях генной терапии. Проведение данного испытания дарит надежду пациентам с таким заболеванием, и что возможно в будущем их качество жизни улучшится.»
— добавила она.
ПКМДR9 вызвана мутациями в гене FKRP. AB-1003, также известная, как LION-101, разработана как средство доставки здоровой копии поврежденного гена непосредственно в «тело» клетки посредством инфузии прямо в кровоток. Терапия доставляет этот генетический «груз» через специально разработанный вирусный вектор, который также называют адено-ассоциированным вирусом или ААВ.
«В то время как наследственная природа ПКМД указывает нам на то, что мутация в гене FKRP не может производить нормальный белок FKRP для мышечной функции, AB-1003 имеет своей целью внедрить нормальный FKRP-ген в мышцы, чтобы затем вырабатывать необходимое количество одноименного протеина. Этот подход показал эффективность на доклинических стадиях испытаний на мышиной модели,»
— об этом сообщает Nicholas Johnson, доктор наук в Медицинской школе Университета Содружества Вирджинии.
Исследования GT FP 100 в России
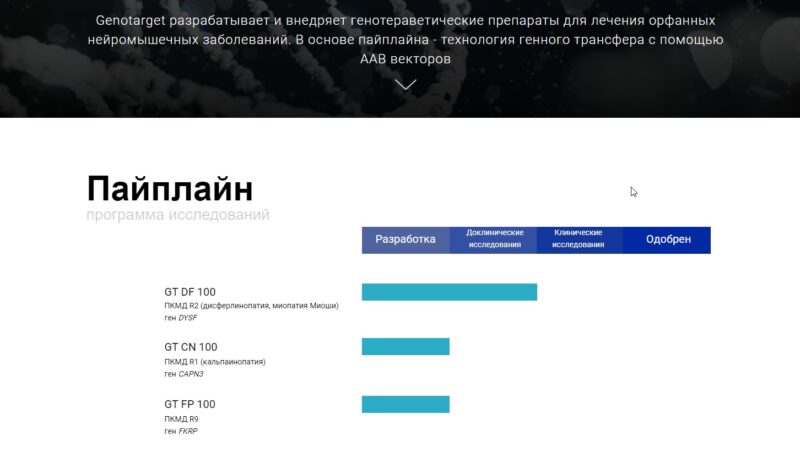
В России разработкой терапии GT FP 100 со схожим механизмом действия занимается компания Genotrget . С учетом этого, можно предположить, что данный подход действительно приведет к появлению лечения для пациентов с поломкой в гене FKRP, и что немаловажно в Российской Федерации. Чтобы быть в курсе новостей о работе Genotarget, рекомендуем подписаться на телеграм-канал компании.
В рамках испытания LION-CS101 ведется набор пациентов в штатах: Вирджиния, Айова и Калифорния
Johnson является ведущим исследователем в фазе 1/2 клинического испытания LION-CS101 (NCT05230459). Для испытания ведутся поиски по привлечению 14 пациентов с ПКМДR9. Участникам будут вводить AB-1003 в одной из двух дозировок или плацебо. Затем, в течение года их состояние будет отслеживаться. Главная цель испытания — установить какой профиль безопасности у экспериментального лечения.
Для участия в испытании LION-CS101 в настоящее время AskBio набирает взрослых людей с верифицированным диагнозом ПКМДR9 на площадках в штатах: Вирджиния, Айова и Калифорния.
«Это испытание является первым шагом по направлению к оценке безопасности AB-1003 и определению возможностей терапии, способной улучшить жизнь пациентов с таким жизнеугрожающим, наследственным и крайне редким заболеванием».
— сказал Johnson.
Терапия AB-1003 в прошлом году получила статус препарата для орфанных заболеваний в Европейском союзе. В 2021 году терапия приобрела статус ускоренного рассмотрения от FDA.
AskBio является дочерней компанией и принадлежит Bayer AG. Компании работают независимо друг от друга. AB-1003 является разработкой Viralgen, которая тоже в свою очередь принадлежит AskBio, являясь дочерним предприятием последней.
