02.06.2020 ReveraGen BioPharma завершили лечение 41 пациента с Мышечной дистрофией Дюшенна (МДД) препаратом Vamorolone. Срок терапии 2,5 года.
Собранные в течение продолжительного времени данные исследования показали, что прием даже высоких доз препарата Vamorolone был безопасен и хорошо переносим. Серьезных побочных эффектов отмечено не было. Предварительные данные показали, что Vamorolone может не иметь тех побочных эффектов, как у Prednison. Как оказалось, Vamorolone показал идентичную или даже более высокую эффективность.
О мышечной дистрофии Дюшенна
Мышечная дистрофия Дюшенна (МДД) — генетическое заболевание, вызванное мутацией в гене дистрофина на X-хромосоме. Это приводит к отсутствию выработки дистрофина — незаменимого белка для поддержания целостности мышечных клеток. Лечение МДД на данный момент только симптоматическое и направлено на снижение прогрессирования заболевания.
Стандарт поддерживающей терапии МДД — это лечение кортикостероидами. Оно позволяет улучшать функционирование мышц. Тем не менее, продолжительное применение терапии может привести к негативным побочным эффектам. Например, к замедлению роста, что пагубно влияет на качество жизни пациента.
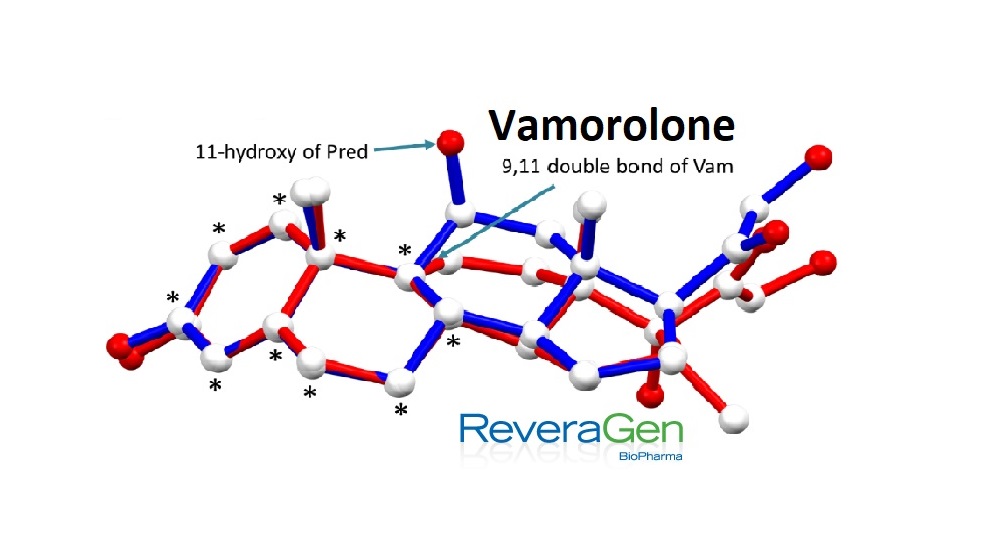
Vamorolone
Vamorolone — это синтетический стероид, который связывается с теми же рецепторами, что и кортикостероиды, но не активирует те же нижестоящие генные пути в клетке. Таким образом, предполагается, что Vamorolone вызывает меньше побочных эффектов, чем кортикостероидная терапия.
Об исследовании
В 2016 году, во вторую фазу исследований (а) привлекли 48 пациентов с МДД (мальчики от 4 до 7 лет). Сообщество клинических исследований Cooperative International Neuromuscular Research Group (CINRG) выступило организатором. Это было четырех-недельное исследование, в котором Vamorolone принимали по одной или по четыре дозы за две недели. Далее, запланированный второй этап отмены препарата в течение двух недель. Основные выводы были следующими: vamorolone может рассматриваться как безопасный препарат. Он усваивается организмом аналогично обычным кортикостероидам. Кроме того, расширение фазы исследований 2 (а) на 6 месяцев показало, что высокие дозы vamorolone привели к более значимым улучшениям в мышечной силе и выносливости. При этом, побочные эффекты были ниже, чем у кортикостероидов.
После продления второй фазы исследования (а) на 6 месяцев большинство пациентов, их семьи и лечащие врачи пожелали продолжить лечение vamorolone. Тогда было принято решение о продлении испытания на 2 года. Пациентам предоставили право выбора получать различные дозы Vamorolone . Примечательно, что все пациенты перешли на более высокие дозы. Однако большинство из них выбрали максимально высокую дозу.
На данный момент, все участники расширенного исследования завершили 18 месячное лечение препаратом Vamorolone. Они продолжают показывать улучшения без подобных кортикостероидам побочных эффектов. Исследование пока еще проводится. Проведено лечение 41 пациента длительностью в 2,5 года. Ожидается, что данные об эффективности будут опубликованы на предстоящих научных конференциях. Большинство из 41 пациентов продолжают лечение посредством расширенной программы доступа (Канада, США и Израиль) и программы благотворительного применения препарата (Великобритания, Швеция и Австралия). Помимо этого, от имени проекта Ай-Мио мы решили запросить информацию у Reveragen о планах создания таких программ на территории Российской Федерации. Информация будет опубликована позднее.
ReveraGen BioPharma инициировали исследование Vamorolone в 2018 году по образцу третьей фазы исследования, которое на данный момент набирает пациентов с МДД (от 4 до 7 лет). Исследование будет определять безопасность и эффективность лечения в сравнении с плацебо и кортикостероидами периодом в 6 месяцев.
Дополнительная информация
Для дополнительной информации по исследованию второй фазы (b), рекомендуем ознакомиться с пресс релизом компании.
[embeddoc url=»https://i-mio.org/app/uploads/2020/06/ReveraGen-Completion-of-LTE-study-2-June-2020-1.pdf» viewer=»google» ]
Чтобы узнать больше о третьей фазе испытаний, посетите сайт ClinicalTrials.gov и введите NCT03439670 в строке поискового запроса.
Источник – “ReveraGen BioPharma Announces Completion of Vamorolone Study in 41 DMD Patients”, SUJATHA GURUNATHAN, Muscular dystrophy association
Выбор, перевод на русский язык и адаптация статьи: Бережной Дмитрий, Чернец Екатерина